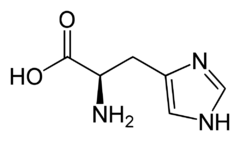
Histidin
Z Multimediaexpo.cz
m (Nahrazení textu) |
(+ Vylepšení) |
||
| (Není zobrazena jedna mezilehlá verze.) | |||
| Řádka 2: | Řádka 2: | ||
| colspan="2" align="center" bgcolor="fefe00"| <font size=+1>'''Histidin'''</font> | | colspan="2" align="center" bgcolor="fefe00"| <font size=+1>'''Histidin'''</font> | ||
|- | |- | ||
| - | | | + | | colspan="2" align="center" |[[Soubor:Histidin - Histidine.png|200px|Struktura Histidinu]]<br /><br />[[Soubor:L-histidine-3D-sticks2.png|180px|Struktura Histidinu]] |
|- | |- | ||
|Systematický název||kyselina 2-amino-3-(1H-imidazol-4-yl) [[propan]]ová | |Systematický název||kyselina 2-amino-3-(1H-imidazol-4-yl) [[propan]]ová | ||
| Řádka 14: | Řádka 14: | ||
|[[Molární hmotnost]]|| 155,16 g/mol | |[[Molární hmotnost]]|| 155,16 g/mol | ||
|} | |} | ||
| - | '''Histidin''' (zkratky '''His''' nebo '''H''') je jedna z nejběžnějších přírodních [[Aminokyseliny|aminokyselin]] přítomných v [[protein]]ech. Ve smyslu [[Výživa|výživy]] je u člověka považován histidin jako [[esenciální aminokyselina]], ale většinou jen u dětí. Jeho [[kodón]]y jsou CAU a CAC. | + | '''Histidin''' (zkratky '''His''' nebo '''H''') je jedna z nejběžnějších přírodních [[Aminokyseliny|aminokyselin]] přítomných v [[protein]]ech. Ve smyslu [[Výživa|výživy]] je u člověka považován histidin jako [[esenciální aminokyselina]], ale většinou jen u dětí. |
| - | Histidin byl poprvé izolován [[Německo|německým]] lékařem | + | |
| - | + | Jeho [[kodón]]y jsou CAU a CAC. | |
| + | |||
| + | Histidin byl poprvé izolován [[Německo|německým]] lékařem Albrechtem Kosselem (1853–1927) v roce 1896. | ||
| + | |||
==[[Metabolismus]]== | ==[[Metabolismus]]== | ||
V lidském těle funguje histidin jako [[prekurzor (chemie)|prekurzor]] pro výrobu [[histamin]]u a [[karnosin]]u. | V lidském těle funguje histidin jako [[prekurzor (chemie)|prekurzor]] pro výrobu [[histamin]]u a [[karnosin]]u. | ||
| - | + | ||
Enzym [[lyáza histidinu]] přeměňuje histidin na [[amoniak]] a [[kyselina urokanová|kyselinu urokanovou]]. Nedostatek tohoto enzymu se projevuje ve vzácné [[metabolismus|metabolické]] poruše [[histidinemie|histidinemii]]. | Enzym [[lyáza histidinu]] přeměňuje histidin na [[amoniak]] a [[kyselina urokanová|kyselinu urokanovou]]. Nedostatek tohoto enzymu se projevuje ve vzácné [[metabolismus|metabolické]] poruše [[histidinemie|histidinemii]]. | ||
| + | |||
| + | <gallery widths="240px" heights="240px"> | ||
| + | Soubor:Histidine-decarboxylase.png|Přeměna histidinu na [[histamin]] účinkem [[enzym]]u [[histidin dekarboxyláza]] | ||
| + | Soubor:D-Histidine.png|D-histidin | ||
| + | </gallery> | ||
== Další články == | == Další články == | ||
* [[seznam kyselin]] | * [[seznam kyselin]] | ||
Aktuální verze z 17. 11. 2016, 01:13
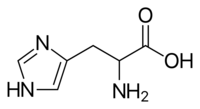
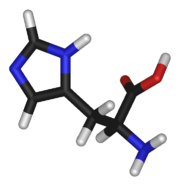
| Histidin | |
| |
| Systematický název | kyselina 2-amino-3-(1H-imidazol-4-yl) propanová |
| Triviální název | histidin |
| Registrační číslo CAS | 71-00-1 |
| Sumární vzorec | C6H9N3O2 |
| Molární hmotnost | 155,16 g/mol |
Histidin (zkratky His nebo H) je jedna z nejběžnějších přírodních aminokyselin přítomných v proteinech. Ve smyslu výživy je u člověka považován histidin jako esenciální aminokyselina, ale většinou jen u dětí.
Jeho kodóny jsou CAU a CAC.
Histidin byl poprvé izolován německým lékařem Albrechtem Kosselem (1853–1927) v roce 1896.
Metabolismus
V lidském těle funguje histidin jako prekurzor pro výrobu histaminu a karnosinu.
Enzym lyáza histidinu přeměňuje histidin na amoniak a kyselinu urokanovou. Nedostatek tohoto enzymu se projevuje ve vzácné metabolické poruše histidinemii.
Přeměna histidinu na histamin účinkem enzymu histidin dekarboxyláza |
Další články
Externí odkazy
|
| Aminokyseliny |
|---|
|
Alanin • Arginin • Asparagin • Cystein • Fenylalanin • Glutamin • Glycin • Histidin • Isoleucin • Kyselina asparagová • Kyselina glutamová • |
| Speciální aminokyseliny |
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |