Návštěvnost dne 8. března 2026 byla — 612 557 unikátních návštěvníků !
Návštěvnost dne 9. března 2026 byla — 590 729 unikátních návštěvníků !
Návštěvnost dne 10. března 2026 byla — 657 697 unikátních návštěvníků !
Tellur
Z Multimediaexpo.cz
| Tellur | |
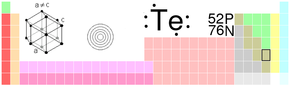
| |
| Atomové číslo | 52 |
| Relativní atomová hmotnost | 127,60(3) amu |
| Elektronová konfigurace | [Kr] 4d10 5s2 5p4 |
| Elektronegativita (Pauling) | 2,1 |
| Teplota tání | 449,51 °C (722,66 K) |
| Teplota varu | 988 °C (1261 K) |
| Hustota | 6,24 g.cm-3 |
| Hustota při teplotě tání | 5,70 g.cm-3 |
| Registrační číslo CAS | 13494-80-9 |
| Tvrdost | 2,25 |
Tellur, chemická značka Te, lat. Tellurium je polokovový stříbřitě lesklý prvek za skupiny chalkogenů používaný v polovodičové technice a metalurgii
Obsah |
Základní fyzikálně - chemické vlastnosti
Tellur je dosti vzácný prvek, byl objeven roku 1782 Franzem Josephem Mullerem. Chemicky patří spíše mezi kovy, ale jsou známy i kyseliny telluru a jejich soli, v nichž chemicky připomíná spíše síru nebo selen.
Výskyt, výroba
Tellur obvykle doprovází síru a selen v jejich rudách. Má značnou afinitu ke zlatu a v mnoha zlatých ložiscích se vyskytuje jako příměs. Z minerálů jsou známy například tellurid zlata calaverit AuTe2 nebo tellurid olova altait PbTe. Průmyslově se tellur získává nejčastěji z anodových kalů po elektrolytické výrobě mědi nebo ze zbytků po rafinaci zlata. Relativní zastoupení telluru v zemské kůře je velmi nízké. Odhaduje se, že jeho obsah kolísá v rozmezí 0,001–0,005 ppm (mg/kg). V mořské vodě je jeho koncentrace tak nízká, že současné analytické techniky nebyly schopny jeho množství spolehlivě změřit.
Sloučeniny a využití
Elementární tellur je za normálních podmínek stálý stříbřitě lesklý a poměrně křehký kov. Dosti snadno se slučuje s kyslíkem a halogeny. Ve sloučeninách se tellur vyskytuje v mocenství Te2-, Te2+, Te4+ a Te6+ . V metalurgii složí tellur ve formě mikrolegur ke zlepšování mechanických a chemických vlastností slitin. Nízké koncentrace telluru zvyšují tvrdost a pevnost slitin olova i jejich odolnost vůči působení kyseliny sírové. Přídavky telluru do slitin mědi a nerezových ocelí způsobují jejich snazší mechanickou opracovatelnost. Telurid gallia nalézá využití v polovodičovém průmyslu. Pro výrobu některých termoelektrických zařízení se používá tellurid bismutu. Ve sklářském průmyslu je v některých speciálních případech tellurem barveno sklo. Jako velmi perspektivní se jeví použití sloučenin telluru při výrobě fotočlánků. Fotočlánky na bázi telluridu kadmia patří v současné době k nejvýkonnějším a probíhá intenzivní výzkum s cílem vyrobit prakticky využitelné solární panely. Na bázi teluridů jsou i záznamové vrstvy v přepisovatelných optických discích. Z hlediska působení na lidské zdraví patří sloučeniny telluru mezi toxické a především v průmyslových provozech, kde se vyskytují ve zvýšených koncentracích je třeba zachovávat přísné bezpečnostní předpisy. Za zvláště nebezpečné je pokládáno vdechování aerosolů a prachu s vysokou koncentrací telluru.
Literatura
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood - A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Externí odkazy
- Periodická soustava a tabulka vlastností prvků [1]
- Chemický vzdělávací portál [2]
- WebElements (anglicky) [3]
- Periodická tabulka prvků [4]
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |

