Multimediaexpo.cz je již 18 let na českém internetu !!
Thallium
Z Multimediaexpo.cz
(→Externí odkazy: Vylepšení) |
m (1 revizi) |
Aktuální verze z 22. 10. 2013, 13:42
| Thallium | |
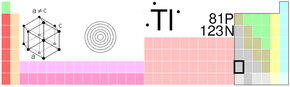
| |
| Atomové číslo | 81 |
| Relativní atomová hmotnost | 204,3833(2) amu |
| Elektronová konfigurace | [Xe] 4f14 5d10 6s2 6p1 |
| Elektronegativita (Pauling) | 1,62 |
| Teplota tání | 304 °C (577 K) |
| Teplota varu | 1473 °C (1746 K) |
| Hustota | 11,85 g.cm-3 |
| Hustota při teplotě tání | 11,22 g.cm-3 |
| Registrační číslo CAS | 7440-28-0 |
| Tvrdost | 1,2 |
Thallium, chemická značka Tl, lat. Thallium je značně toxický měkký, lesklý kov bílé barvy.
Obsah |
Základní fyzikálně - chemické vlastnosti
Velmi řídce se vyskytující kovový prvek, nalézající se obvykle jako příměs v sulfidických rudách. V přírodě se vyskytuje pouze ve formě sloučenin, v mocenství Tl+1 a Tl+3. Objevil jej roku 1861 sir William Crookes při spektroskopickém zkoumání obsahu telluru ve zbytcích po zpracování sulfidických rud.
Výskyt a výroba
- Thallium je v zemské kůře značně vzácným prvkem. Průměrný obsah činí pouze 0,5-2 ppm (mg/kg). V mořské vodě je jeho koncentrace natolik nízká, že ji nelze změřit ani nejcitlivějšími analytickými technikami, udává se, že je nižší než 0,01 μg/l. Ve vesmíru připadá na jeden atom thallia přibližně 300 miliard atomů vodíku.
- V horninách se vyskytuje vždy pouze jako příměs, především v sulfidických rudách mědi, olova a zinku. Odpad po zpracování těchto rud slouží pak jako surovina pro přípravu čistého thallia elektrolýzou. V některých lokalitách se také nachází ve zvýšené koncentraci v jílových minerálech a žule.
Využití
- Většina produkce se spotřebovává v elektronice. Je důležitým prvkem při výrobě některých polovodičů, např. tranzistorů, fotočlánků s citlivostí v infračervené oblasti spektra, a supravodičů.
- Sloučeniny thalia jsou značně toxické, a používají se proto jako základní součást některých prostředků na hubení krys, dalších hlodavců i hmyzu, za což si tyto přípravky zasloužili neblahou kritiku.
- Thallium nachází uplatnění při výrobě speciálních skel. Jde o slitiny se sírou, selenem a arzenem, které poskytují velmi těžká, ale snadnou tavitelná (teplota tání 125-150 °C) skla s mimořádně velkou odrazivostí, tedy s vysokým lomem světla.
- Přidává se do lehkotavitelných slitin.
- Výbojky plněné parami thallia vydávají zelené světlo.
- Jeho slabými roztoky se impregnuje dřevo a moří obilí před výsevem.
- Slouží k výrobě detekčních členů pro měření úrovně gama radiace v atomových elektrárnách a jaderném výzkumu.
Zdravotní rizika
Thallium je považováno za mimořádně toxický prvek. V mnoha státech světa proto již bylo zakázáno používat jej jako součást nástrah na krysy a mravence. V hutním a metalurgickém průmyslu hrozí expozice pracovníků thalliem v poletavém prachu. Jako maximální přípustná dávka bylo určeno množství 0,1 mg Tl na 1 m2 pokožky za pracovní směnu. Při dlouhodobějším styku se solemi thalia dochází k vypadávání vlasů a soli thalia jsou pokládány za potenciálně karcinogenní. Thallium postihuje periferní nervy a později jed poškozuje mozkové centrum a vnitřní orgány. Smrtelná dávka je menší než jeden gram, avšak lékaři již dnes znají protilátku, kterou je pruská modř. Pro tyto vlastnosti je thallium oblíbené mezi traviči.
Literatura
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood - A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Externí odkazy
- Periodická soustava a tabulka vlastností prvků [1]
- Chemický vzdělávací portál [2]
- WebElements (anglicky) [3]
- Periodická tabulka prvků [4]
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |


