Návštěvnost dne 25. února 2026 byla — 484 927 unikátních návštěvníků !
Návštěvnost dne 26. února 2026 byla — 479 665 unikátních návštěvníků !
Návštěvnost dne 5. března 2026 byla — 475 445 unikátních návštěvníků !
Erbium
Z Multimediaexpo.cz
| Erbium | |
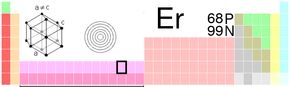
| |
| Atomové číslo | 68 |
| Relativní atomová hmotnost | 167,259(3) amu |
| Elektronová konfigurace | [Xe] 4f12 6s2 |
| Skupenství | Pevné |
| Teplota tání | 1529 °C, (1802 K) |
| Teplota varu | 2868 °C, (3141 K) |
| Elektronegativita (Pauling) | 1,24 |
| Hustota | 9,066 g/cm3 |
| Hustota při teplotě tání | 8,86 g/cm3 |
| Registrační číslo CAS | 7440-52-0 |
| Vzhled | |
| Atomový poloměr | 1,75 Å (175 pm) |
| Výparné teplo | 280 kJ/mol |
| Skupenské teplo tání | 19,90 kJ/mol |
| Tepelná kapacita | 28,12 J.mol-1.K-1 |
| Ionisační energie Er→Er+ | 589,3 kJ/mol |
| Ionisační energie Er+→Er2+ | 1150 kJ/mol |
| Ionisační energie Er2+→Er3+ | 2194 kJ/mol |
Erbium, chemická značka Er, (lat. Erbium) je měkký stříbřitě bílý, přechodný kovový prvek, 12. člen skupiny lanthanoidů. Nachází využití při výrobě speciálních slitin pro jadernou energetiku a ve sklářském a keramickém průmyslu.
Obsah |
Základní fyzikálně-chemické vlastnosti
Erbium je stříbřitě bílý, měkký přechodný kov.
Chemicky je erbium méně reaktivní než předchozí prvky ze skupiny lanthanoidů. Na suchém vzduchu je prakticky stálé, ve vlhkém prostředí se pomalu pokrývá vrstvičkou oxidu. Snadno se rozpouští v běžných minerálních kyselinách za vývoje vodíku.
Ve sloučeninách se vyskytuje pouze v mocenství Er+3. Soli Er+3 vykazují vlastnosti podobné sloučeninám hliníku a ostatních lanthanoidů. Všechny tyto prvky tvoří například vysoce stabilní oxidy, které nereagují s vodou a jen velmi obtížně se redukují. Ze solí anorganických kyselin jsou důležité především fluoridy a fosforečnany, jejich nerozpustnost ve vodě se používá k separaci lanthanoidů od jiných kovových iontů. Erbité soli mají obvykle červenou nebo narůžovělou barvu.
Erbium objevil roku 1843 švédský chemik Carl Gustaf Mosander v minerálu gadolinitu, avšak čistý elementární kov byl připraven až v roce 1943. Jméno dostalo erbium podle vesnice Ytterby, švédské vesnice, poblíž které bylo poprvé nalezeno.
Výskyt a výroba
Erbium je v zemské kůře obsaženo v koncentraci přibližně 2,6 mg/kg, o jeho obsahu v mořské vodě údaje chybí. Ve vesmíru připadá jeden atom erbia na 100 miliard atomů vodíku.
V přírodě se erbium vyskytuje pouze ve formě sloučenin. Neexistují však ani minerály, v nichž by se některé lanthanoidy (prvky vzácných zemin) vyskytovaly samostatně, ale vždy se jedná o minerály směsné, které obsahují prakticky všechny prvky této skupiny. Mezi nejznámější patří monazity (Ce, La, Th, Nd, Y)PO4 a xenotim, chemicky fosforečnany lanthanoidů, dále bastnäsity (Ce, La, Y)CO3F– směsné flourouhličitany prvků vzácných zemin a např. minerál euxenit (Y,Ca,Ce,U,Th)(Nb,Ta,Ti)2O6.
Velká ložiska těchto rud se nalézají ve Skandinávii, USA, Číně a Vietnamu. Významným zdrojem jsou i fosfátové suroviny - apatity z poloostrova Kola v Rusku
Při průmyslové výrobě prvků vzácných se jejich rudy nejprve louží směsí kyseliny sírové a chlorovodíkové a ze vzniklého roztoku solí se přídavkem hydroxidu sodného vysráží hydroxidy.
Separace jednotlivých prvků se provádí řadou různých postupů – kapalinovou extrakcí, za použití ionexových kolon nebo selektivním srážením nerozpustných komplexních solí.
Příprava čistého kovu se obvykle provádí redukcí fluoridu erbitého ErF3 elementárním vápníkem.
- 2 ErF3 + 3 Ca → 2 Er + 3 CaF2
Použití a sloučeniny
- Podobně jako gadolinium a holmium, vykazuje erbium vysoký účinný průřez pro záchyt tepelných neutronů a jeho slitiny jsou materiálem pro výrobu moderátorových tyčí v jaderných reaktorech. Zasunutím těchto tyčí do nitra rektoru dojde k poklesu neutronového toku a tím zpomalení štěpné reakce.
- V metalurgickém průmyslu se přídavky erbia do slitin vanadu zlepšují jejich mechanické vlastnosti – snižují jejich tvrdost a přispívají k lepší opracovatelnosti slitků.
- Sloučeniny erbia se ve sklářském a keramickém průmyslu užívají pro barvení skloviny a glazur do červena a růžova.
- Některé vláknové lasery pracující v pulsním režimu jsou založeny na použití optického vlákna dotovaného erbiem.
Literatura
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood - A. Earnshaw, Chemie prvků II. 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Externí odkazy
- Periodická soustava a tabulka vlastností prvků [1]
- Chemický vzdělávací portál [2]
- WebElements (anglicky) [3]
- Periodická tabulka prvků [4]
|
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |

