Návštěvnost dne 8. března 2026 byla — 612 557 unikátních návštěvníků !
Návštěvnost dne 9. března 2026 byla — 590 729 unikátních návštěvníků !
Návštěvnost dne 10. března 2026 byla — 657 697 unikátních návštěvníků !
Plutonium
Z Multimediaexpo.cz
| Plutonium | |
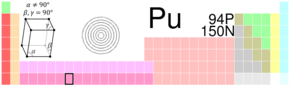
| |
| Atomové číslo | 94 |
| Relativní atomová hmotnost | (244) amu |
| Elektronová konfigurace | [Rn] 5f6 7s2 |
| Skupenství | Pevné |
| Teplota tání | 639,4 °C, (912,5 K) |
| Teplota varu | 3228 °C, (3505 K) |
| Elektronegativita (Pauling) | 1,28 |
| Hustota | 19,816 g/cm3 |
| Hustota při teplotě tání | 16,63 g/cm3 |
| Registrační číslo CAS | 7440-07-5 |
| Vzhled | |
| Atomový poloměr | 1,75 Å (175 pm) |
| Výparné teplo | 333,5 kJ/mol |
| Skupenské teplo tání | 2,82 kJ/mol |
| Tepelná kapacita | 35,5 J.mol-1.K-1 |
| Ionizační potenciál Pu→Pu+ | 584,7 kJ/mol |
Plutonium, chemická značka Pu, (lat. Plutonium) je šestý člen z řady aktinoidů, druhý transuran, silně radioaktivní, velmi toxický kovový prvek, připravovaný uměle v jaderných reaktorech především pro výrobu atomových bomb. Je využitelné rovněž jako palivo pro jaderné reaktory a jako zdroj energie pro radioizotopový termoelektrický generátor.
Obsah |
Základní fyzikálně-chemické vlastnosti
Plutonium je radioaktivní kovový prvek stříbřitě bílé barvy, která se působením vzdušného kyslíku mění na šedavou. Ve sloučeninách se vyskytuje v mocenství od Pu+3 po Pu+7, přičemž stálejší jsou sloučeniny s nižší valencí. Soli plutonia vykazují v roztoku rozdílné zabarvení podle mocenství plutoniového iontu. Čistý kov lze připravit redukcí fluoridu plutonia kovovým lithiem nebo baryem při teplotě kolem 1200 °C.
Historie objevu
Plutonium bylo poprvé připraveno roku 1940 dvěma vědeckými týmy bombardováním 238U neutrony. V jaderné laboratoři v Berkeley na kalifornské univerzitě ho připravili Edwin M. McMillan a Philip Abelson a v britské Cambridgi ohlásili jeho přípravu Norman Feather a Egon Bretscher. Příprava a izolace čistého kovu se uskutečnila 23. února 1941 v Berkeley bombardováním uranu jádry deuteria v cyklotronu. Jako autoři tohoto experimentu jsou označováni Glenn T. Seaborg, Edwin McMillan, J. W. Kennedy, a A. C. Wahl. Vzhledem k probíhající druhé světové válce byly výsledky tohoto bádání udržovány v tajnosti, zvláště proto, že jedna ze dvou atomových bomb svržených USA na Japonsko byla vyrobena právě z plutonia.
Výskyt a izotopy
Plutonium patří mezi uměle připravené prvky a v přírodě je možné se setkat jen se skutečně ultrastopovými množstvími v uranových rudách, kde mohou jednotlivé atomy vzniknout z 238U po záchytu neutronu a následných dvou rozpadech β. Mezi přibližně 20 známými izotopy plutonia existuje několik, které vykazují dostatečně velký poločas rozpadu, aby je bylo možno prakticky využít. Nejdelší poločas (asi 80 milionů let) má 244Pu, nejdůležitější izotop 239Pu se rozpadá s poločasem 24 100 let, 240Pu 6500 let, 241Pu 14 roků, 242Pu 373 000 let a 238Pu má poločas rozpadu 88 let; existuje však celá řada dalších izotopů. Všechny uvedené izotopy jsou zářiče α, pouze 240Pu se chová jako zářič β.
Výroba a využití
Jaderné zbraně
Plutonium je od 40. let 20. století nejvíce vyráběným umělým prvkem a to především proto, že izotop 239Pu je vhodný pro výrobu atomové bomby. Stejně jako v případě 235U dochází při nahromadění větších kvant čistého izotopu k nastartování řetězové štěpné reakce, kdy po rozpadu jednoho atomového jádra vznikají obvykle tři neutrony, které působí rozpady dalších okolních jader a rozpad se nekontrolovaně rozrůstá. Kritické množství čistého kovového plutonia 239Pu je přibližně 16 kg, s použitím neutronového odrážeče lze toto množství snížit až na 10 kg. Plutoniová jaderná puma má sílu výbuchu přibližně 20 kt TNT na každý kilogram použitého plutonia. Princip výroby 239Pu spočívá v reakci 238U s neutronem za vzniku 239U v jaderném reaktoru. Jádro 239U je značně nestabilní a rozpadem β rychle vzniká izotop neptunia 239Np, jež se opět rychle dalším β-rozpadem mění na 239Pu. Tento izotop plutonia se chová jako α zářič a relativně snadno se dále zpracovává.
- 23892U + 10n → 23992U → 23993Np + 0-1e → 23994Pu + 0-1e
Při výrobě izotopu 238Pu se uran 238U bombarduje jádry deuteria:
- 23892U + 21D → 23893Np + 2 10n → 23894Np + 0-1e
V případě, že jádro 239Pu zachytí další neutron, dojde k jeho přeměně na 240Pu. Tento izotop je z hlediska další manipulace a zpracování rizikový protože je β–zářičem a zároveň není vhodný pro výrobu atomové zbraně. Protože izotopy 239Pu a 240Pu lze jen velmi obtížně oddělovat, je při výrobě 239Pu z 238U v jaderném reaktoru nutno pečlivě volit dobu setrvání 238U v reaktoru. Při dlouhodobém ozařování sice roste množství 239Pu, ale současně narůstá i podíl nechtěného izotopu 240Pu. Na druhé straně je ekonomicky značně nákladné oddělovat izotopy plutonia od zbytku jaderného paliva z reaktoru a je proto otázkou komplikovaných výpočtů určit, v jakém stádiu výroby má být reakce přerušena a materiál chemicky přepracován na čisté plutonium. Další důležitou proměnnou veličinou je zde pochopitelně i procentuální vsázka 238U do jaderné reakce.
Další využití
- Podobně jako v případě uranu, může být řetězová reakce, v níž po záchytu neutronu dojde k rozpadu atomového jádra prvku za uvolnění dalších neutronů a kinetické energie štěpných produktů, využita i pro výrobu energie v upravených jaderných reaktorech. V současné době pracuje na světě několik jaderných reaktorů na bázi směsi 239Pu a 240Pu, obecně jsou však tyto reaktory pokládány za méně bezpečné než klasické uranové vzhledem k vysoké toxicitě plutonia a jeho sloučenin.
- Izotop 238Pu s poločasem rozpadu 88 let slouží často jako energetický zdroj především v kosmických sondách. V tzv. radioizotopovém termoelektrickém generátoru se mění tepelná energie uvolněná samovolným jaderným rozpadem na elektrickou pomocí termočlánků. Pro tyto účely jsou vhodné izotopy s poločasem rozpadu v řádu desítek let, protože uvolněná energie je dostatečně velká, aby mohla být prakticky využita a zároveň zaručuje použitelnost zdroje po dobu minimálně 50 let. Produkovaný výkon generátoru dosahuje stovek wattů, což postačuje pro udržení provozu základních elektrických přístrojů vesmírné sondy. Plutoniové generátory zásobují energií např. sondy Galileo nebo Cassini a udržují v provozu vědecké přístroje, zanechané na Měsíci kosmonauty v rámci projektu Apollo.
- Spíše jako zajímavost může sloužit informace, že výše uvedené generátory elektrické energie v některých případech slouží jako energetický zdroj pro pacemakery, medicínské přístroje sloužící ke zklidnění srdečního rytmu u osob s rizikem infarktu. V současné době jsou pro tyto účely používány především lithiové baterie s dlouhou životností a indukčním dobíjením, ale před jejich vynálezem byl energetický zdroj fungující na principu jaderného rozpadu 238Pu přijatelnou alternativou.
Zdravotní rizika
Plutonium je jako těžký kov toxické chemicky, v praxi lze však u něho těžko rozlišit škodlivé účinky způsobené radiací od škodlivých účinků chemických; je často pokládáno za jednu z nejtoxičtějších anorganických látek. Podle některých údajů můžou být už mikrogramová množství tohoto prvku smrtelně jedovatá pro člověka, pokud se dostanou do krevního oběhu. Jiné zdroje však tvrzení o extrémní toxicitě kovového plutonia považují za tendenčně nadhodnocené a používané především skalními odpůrci využití jaderné energetiky. J. Marhold cituje z prací, kde je uvedena DL50 u psa i.v. 0,3mg/kg, u myši i.p. 1750mg/kg. Evidentně tedy nejde o látku akutně extrémně toxickou. Za hlavní nebezpečí se považuje depozice v kostech. Radiačně nebezpečný je především izotop 240Pu, který jako β-zářič má daleko negativnější dopad na lidské zdraví než zbylé izotopy plutonia, zářiče α. Je pochopitelné, že mimořádné nebezpečí by hrozilo při nastartování řetězové štěpné reakce, kdy se plutonium stává zdrojem silného neutronového toku. K tomu však může dojít pouze při neopatrné manipulaci s většími objemy čistého plutonia, v počátcích výzkumu plutonia v laboratořích v Berkeley skutečně několikrát došlo k vysoké expozici pracovníků neutrony, konkrétně nehody při experimentech s kritickým množstvím, 21. srpna 1945 nehoda Harryho K. Daghliana Jr. (1921-1945) a 21. května 1946 nehoda Louise P. Slotina (1910-1946). Při těchto nehodách došlo k vysokému ozáření menšího počtu osob, H.K.Daghlian zemřel 26 dní po nehodě, L.P.Slotin po 9 dnech.
Související články
Literatura
- Cotton F.A., Wilkinson J.: Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.: Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood, A. Earnshaw, Chemie prvků II. 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Externí odkazy
- Zdravotní účinky plutonia na itv1.cz (v PDF)
- Petr Otčenášek: Odpady z palivového cyklu jaderných elektráren časopis Vesmír, 84, 536, 2005/9
- Co je smíšené oxidové palivo (MOX) a kde se používá?, Česká nukleární společnost, Zpravodaj 2/2000
- Vladimír Wagner: Jaderná energie pro meziplanetární sondy, astro.cz
- (anglicky) IARC MONOGRAPHS ON THE EVALUATION OF CARCINOGENIC RISKS TO HUMANS, VOLUME 78 IONIZING RADIATION, PART 2: SOME INTERNALLY DEPOSITED RADIONUCLIDES IARC 2001
- WebElements (anglicky)
- Novinky.cz - Izrael vyvinul plutonium, které nelze použít na atomovou bombu
- Chemický vzdělávací portál [1]
- WebElements (anglicky) [2]
- Periodická tabulka prvků [3]
|
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |



