Multimediaexpo.cz je již 18 let na českém internetu !!
Cer
Z Multimediaexpo.cz
m (Nahrazení textu) |
m (1 revizi) |
Aktuální verze z 27. 4. 2014, 11:18
| Cer | |
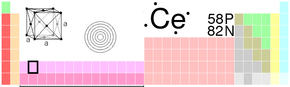
| |
| Atomové číslo | 58 |
| Relativní atomová hmotnost | 140,116(1) amu |
| Elektronová konfigurace | [Xe] 4f1 5d1 6s2 |
| Skupenství | Pevné |
| Teplota tání | 795 °C, (1068 K) |
| Teplota varu | 3443 °C, (3716 K) |
| Elektronegativita (Pauling) | 1,12 |
| Hustota | 6,770 g/cm3 |
| Hustota při teplotě tání | 6,55 g/cm3 |
| Registrační číslo CAS | 7440-45-1 |
| Vzhled | |
| Atomový poloměr | 1,85 Å (185 pm) |
| Výparné teplo | 398 kJ/mol |
| Skupenské teplo tání | 5,46 kJ/mol |
| Ionisační energie Ce→Ce+ | 534,4 kJ/mol |
| Ionisační energie Ce+→Ce2+ | 1050 kJ/mol |
| Ionisační energie Ce2+→Ce3+ | 1949 kJ/mol |
| Tvrdost | 2,5 |
Cer, chemická značka Ce, (lat. Cerium) je šedavě bílý, vnitřně přechodný kovový prvek, druhý člen skupiny lanthanoidů. Hlavní uplatnění nalézá ve metalurgickém průmyslu při výrobě speciálních slitin a nebo jejich deoxidaci, je složkou některých skel a průmyslových katalyzátorů.
Obsah |
Základní fyzikálně-chemické vlastnosti
Cer vzhledově připomíná železo, je to šedavě bílý přechodný kov, který je však značně měkký a snadno tvárný.
Chemicky je cer značně reaktivním prvkem, po europiu nejreaktivnějším lanthanoidem. Za mírně zvýšené teploty (kolem 80 °C) reaguje se vzdušným kyslíkem (hoří) za vzniku velmi stabilního oxidu ceričitého CeO2. S vodou reaguje cer za vzniku plynného vodíku, snadno se rozpouští v běžných minerálních kyselinách.
Ve sloučeninách se vyskytuje v mocenství Ce+3 a jako jediný z lanthanoidů tvoří i stabilní sloučeniny s valencí Ce+4. Soli Ce+3 jsou obvykle bílé, sloučeniny čtyřmocného ceru mají barvu žlutou až oranžovou.
Objevili jej současně roku 1803 švédský chemik Jöns Jacob Berzelius a Wilhelm von Hisinger a zároveň v Německu Martin Heinrich Klaproth.
Výskyt a výroba
Cer je v zemské kůře nejvíce zastoupeným prvkem ze skupiny lanthanoidů – vyskytuje se zde v koncentraci asi 46 - 60 mg/kg. V mořské vodě je jeho koncentrace kolem 0,0004 mg/l. Ve vesmíru připadá jeden atom ceru na 30 miliard atomů vodíku.
V přírodě se cer vyskytuje pouze ve formě sloučenin. Neexistují však ani minerály, v nichž by se některé lanthanoidy (prvky vzácných zemin) vyskytovaly samostatně, ale vždy se jedná o minerály směsné, které obsahují prakticky všechny prvky této skupiny. Mezi nejznámější patří monazity (Ce, La, Th, Nd, Y)PO4 a xenotim, chemicky fosforečnany lanthanoidů a dále bastnäsity (Ce, La, Y)CO3F – směsné flourouhličitany prvků vzácných zemin.
Velká ložiska těchto rud se nalézají ve Skandinávii, USA, Číně a Vietnamu. Významným zdrojem jsou i fosfátové suroviny - apatity z poloostrova Kola v Rusku
Při průmyslové výrobě prvků vzácných se jejich rudy nejprve louží směsí kyseliny sírové a chlorovodíkové a ze vzniklého roztoku solí se přídavkem hydroxidu sodného vysráží hydroxidy.
K separaci ceru od zbylých lanthanoidů se obvykle využívá skutečnosti, že hydroxid ceričitý Ce(OH)4 podléhá hydrolýze již v relativně kyselých roztocích (kolem pH = 2). Směs lanthanoidů se proto nejprve oxiduje působením manganistanu draselného KMnO4, který převede veškerý cer do mocenství Ce+4 a postupnou neutralizací kyselého roztoku se vysráží prakticky čistý nerozpustný hydroxid ceričitý.
Kovový cer se obvykle vyrábí elektrolýzou taveniny směsi chloridu ceritého CeCl3 a chloridu sodného NaCl v grafitové nádobě. Cer se přitom vylučuje na grafitové katodě, zatímco na anodě dochází k uvolňování plynného chloru.
Použití a sloučeniny
Vzhledem k vysokému zastoupení ceru v rudách vzácných zemin je tohoto prvku na trhu relativně nadbytek, protože vzniká částečně jako přebytek při výrobě vysoce žádaných lanthanoidů - především europia nebo samaria .
Základním průmyslové využití nalézá cer v metalurgii.
- Jeho vysoká afinita ke kyslíku a síře se uplatní při odkysličování a desulfuraci vyráběných kovů a slitin.
- Oceli nebo litina s obsahem malých množství ceru vykazují vyšší tvárnost a kujnost a mají vyšší mechanickou odolnost proti nárazu.
- Přídavek ceru do slitin na bázi hořčíku a hliníku zlepšuje jejich odolnost proti teplotním změnám usnadňuje odlévání složitějších výrobků.
- Slitina s wolframem slouží pro výrobu elektrod pro svařování a řezání kovů elektrickým obloukem. Obloukové lampy, sloužící především jako světelné zdroje při natáčení filmů mívají často elektrody ze slitin s obsahem ceru a lanthanu.
Významné uplatnění nalézají sloučeniny ceru, především oxid ceričitý CeO2 ve sklářském průmyslu. Jejich přídavek do skloviny slouží hlavně k odbarvování vyrobeného skla a snižuje jeho propustnost pro ultrafialové záření.
Katalyzátory s obsahem ceru se používají i v petrochemii při krakování ropy.
Brusné a lešticí práškové materiály, používané při výrobě optických součástek (přesné čočky, zrcadla do teleskopů, …) obsahují často významný podíl sloučenin ceru.
Soli čtyřmocného ceru jsou silná oxidační činidla a především síran ceričitý Ce(SO4)2 je často používán v analytické chemii pro oxidaci analyzované látky v redox titracích. Stejně tak nalézá uplatnění v preparativní chemii při oxidační syntéze látek.
Literatura
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood - A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Externí odkazy
- Periodická soustava a tabulka vlastností prvků [1]
- Chemický vzdělávací portál [2]
- WebElements (anglicky) [3]
- Periodická tabulka prvků [4]
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |

