Multimediaexpo.cz je již 18 let na českém internetu !!
Aceton
Z Multimediaexpo.cz
m (Nahrazení textu) |
m (1 revizi) |
Aktuální verze z 13. 12. 2013, 09:19
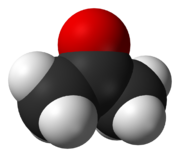
Aceton je triviální pojmenování pro propan-2-on nebo též dimethylketon. Charakteristickou skupinou je karbonyl. Aceton je bezbarvá kapalina specifického zápachu, hořlavá, s vodou neomezeně mísitelná. Směs par s kyslíkem je výbušná. Používá se jako rozpouštědlo organických látek.
Obsah |
Chemické vlastnosti
Aceton je z chemického hlediska zajímavý nejen jako organické rozpouštědlo, ale také jako výchozí surovina syntéz. Reaktivitu acetonu způsobuje přítomnost karbonylové skupiny. Kyslík má větší elektronegativitu než uhlík, a proto tuto vazbu polarizuje tak, že na kyslíku je parciální záporný a na uhlíku parciální kladný náboj. Aceton tedy reaguje s nukleofilními činidly, které mají přebytek elektronů. Tímto způsobem se může adovat například ethanol, voda, kyanid nebo ylid.
Aceton vykazuje také keto-enol tautomerii, i když rovnováha této reakce je výrazně posunuta ve prospěch keto formy. Enol forma se vyskytuje v 6,3x10-6 procentech. Přesto je tento jev, tzv. enolizace, velmi důležitý pro reaktivitu. Díky tomu podléhá aceton například halogenaci či nitrosaci.
Výskyt
V lidském organismu vzniká aceton v malém množství spontánní dekarboxylací acetacetátu, látky, která vzniká v játrech při zpracování mastných kyselin (z tuků). Acetacetát je tzv. ketolátka, která slouží jako alternativní zdroj energie (místo glukózy) pro buňky během hladovění. Aceton je vydýcháván v plicích. Při diabetu se tvoří zvýšené množství ketolátek, proto je dech diabetiků cítit po acetonu.
Výroba
Vyrábí se oxidací (dehydrogenací) isopropanolu, nebo rozkladem octanu vápenatého. Další možností je výroba z kumenu oxidací peroxidem vodíku, ze kterého vzniká kumylhydroperoxid, jenž v kyselém prostředí přesmykuje na aceton a fenol.
Využití v průmyslu
Aceton je základní surovinou chemického průmyslu. Využívá se při syntéze acetonkyanhydrinu, který působením kyseliny sírové přechází na methakrylamid sulfát. Tato sloučenina pak reaguje s methanolem za vzniku methylmetakrylátu - methylesteru kyseliny akrylové. To je základní stavební prvek polymeru známého jako plexisklo. Aceton se také využívá na výrobu podpatků a podrážek a jiných gumových dílů obuvi.
Bezpečnost
Hořlavost
Hlavním nebezpečím spjatým s acetonem je jeho značná hořlavost. Sám se zapálí při teplotě 465 °C. Při teplotách nad zápalným bodem (−20 °C) mohou jeho směsi se vzduchem obsahující 2,5 až 12,8 % acetonu explodovat nebo deflagračně shořet. Páry acetonu mohou téci podél povrchů ke vzdáleným zdrojům zapálení a případný oheň pak šlehne zpět. Páry může zapálit také výboj statické elektřiny.[1]
Peroxidy acetonu
- Hlavní článek: Peroxidy acetonu
Aceton se může oxidovat na velmi nestabilní peroxidy. Může k tomu dojít nechtěně, například pokud se odpadní peroxid vodíku vylije do odpadního rozpouštědla obsahujícího aceton. Peroxidy acetonu jsou více než desetkrát citlivější na tření a náraz než nitroglycerin. Kvůli této nestabilitě se využívají jen zřídka, navzdory snadné syntéze.
Toxikologické vlastnosti
Aceton při běžném použití vykazuje zřejmě jen mírnou toxicitu a neexistují dostatečné důkazy pro chronické účinky na zdraví, dodržují-li se základní zásady.[2] Při velmi vysokých koncentracích par je aceton dráždivý a podobně jako mnoho jiných rozpouštěděl působí tlumivě na centrální nervový systém. Je také velmi dráždivý při kontaktu s očima a při potenciálním vdechnutí kapalného acetonu do plic. V jednom dokumentovaném případě vedlo požití velkého množství acetonu k systémové otravě, ale pacient se nakonec zcela zotavil.[3] Akutní expozice parám o koncentraci cca 4 750 mg/m3 nezpůsobuje významné toxické účinky, objevuje se pouze drobné přechodné postižení, například podráždění očí. U expozic 25 500 mg/m3 po dobu čtyř hodin bylo hlášeno zvracení a poruchy vědomí. Již při koncentracích 595 mg/m3 však docházelo ke změnám ve výsledcích neurobehaviorálních testů, u žen se při koncentraci 2 370 mg/m3 objevovaly menstruační poruchy.[4] Některé zdroje odhahují smrtelnou dávku LD50 pro člověka na 1159 mg/kg (při požití). Čtyřhodinová inhalační LC50 pro myši je 44 g/m3,[5] pro potkany 76 g/m3. Orální LD50 pro potkany je 5800-7138 mg/kg.[4] Je zajímavé, že aceton vykazoval antikonvulzivní účinky na zvířecích modelech epilepsie, aniž by se projevila toxicita, při podávání milimolárních dávek.[6] Proto vznikla hypotéza, že ketogenní dieta s vysokým obsahem tuků a nízkým obsahem sacharidů, používaná klinicky pro léčbu epilepsie rezistentní na léčiva u dětí, účinkuje prostřednictvím zvýšení hladiny acetonu v mozku.[6]
Účinky na životní prostředí
Aceton se rychle vypařuje, a to i z vody a půdy. V atmosféře degraduje působením UV záření s poločasem 22 dnů. V půdě, zvířatech a vodních tocích se šíří pomalu, protože je částečně spotřebováván mikroorganismy.[7] Vzhledem k dobré rozpustnosti ve vodě však může dojít ke kontaminaci spodních vod. Smrtelná koncentrace (LC50) pro ryby je 8,3 g/l (cca 0,8 %) po dobu 96 hodin, poločas v tomto prostředí je 1 až 10 dnů. Aceton může znamenat významné riziko snížení obsahu kyslíku ve vodních systémech, vzhledem k jeho spotřebě mikrobiální aktivitou.[8]
Reference
- ↑ Acetone MSDS
- ↑ http://ccohs.ca/oshanswers/chemicals/chem_profiles/acetone/basic_ace.html
- ↑ Canadian Centre for Occupational Health and Safety. Health Effects of Acetone [online]. [cit. 2008-10-21]. Dostupné online.
- ↑ Chybná citace Chyba v tagu
<ref>; citaci označenéehcnení určen žádný text - ↑ Safety (MSDS) data for propanone
- ↑ 6,0 6,1 Likhodii SS, Serbanescu I, Cortez MA, Murphy P, Snead OC 3rd, Burnham WM. Anticonvulsant properties of acetone, a brain ketone elevated by the ketogenic diet. Ann Neurol., 2003, roč. 54, čís. 2, s. 219–226. DOI:10.1002/ana.10634.
- ↑ tf21
- ↑ http://jmloveridge.com/cosh/Acetone.pdf
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |